2019年11月14日,北京大学白凡研究员团队与广州医科大学附属广州市妇女儿童医疗中心儿科研究所张玉霞研究员,国家临床重点专科儿科消化团队(杨敏、耿岚岚及龚四堂主任医师)合作在《Cell 》以长文形式发表了题为“Mucosal profiling of pediatric-onset colitis and IBD reveals common pathogenic and therapeutic pathways”的研究论文,报道了这一儿童疾病研究领域的重大进展。
1. 队列特征与单细胞转录组图谱
研究团队回顾了2016 ~ 2019年广州医科大学附属广州市妇女儿童医疗中心消化内科招募的306名患儿,并根据临床、生化检验、内镜和组织病理学等评分将患儿分为对照、结肠炎(colitis),溃疡性结肠炎(UC)和克罗恩病(CD)组。结肠炎又分为轻(分级1)、中(分级2)、重度(分级3)三个等级。肠镜时,中-重度结肠炎及UC和CD患者的血红蛋白(HGB)和白蛋白(ALB)显著降低,而超敏C反应蛋白(hsCRP)和血小板计数则升高(图1A-C)。为了阐述致病机制及研究药物靶点,研究团队对17名患儿(包括对照组及PIBD各亚型)的结肠黏膜进行了单细胞转录组及TCR+BCR分析,并将中国儿童的风险基因与各细胞亚型的转录特征进行了关联(图1D-E)。
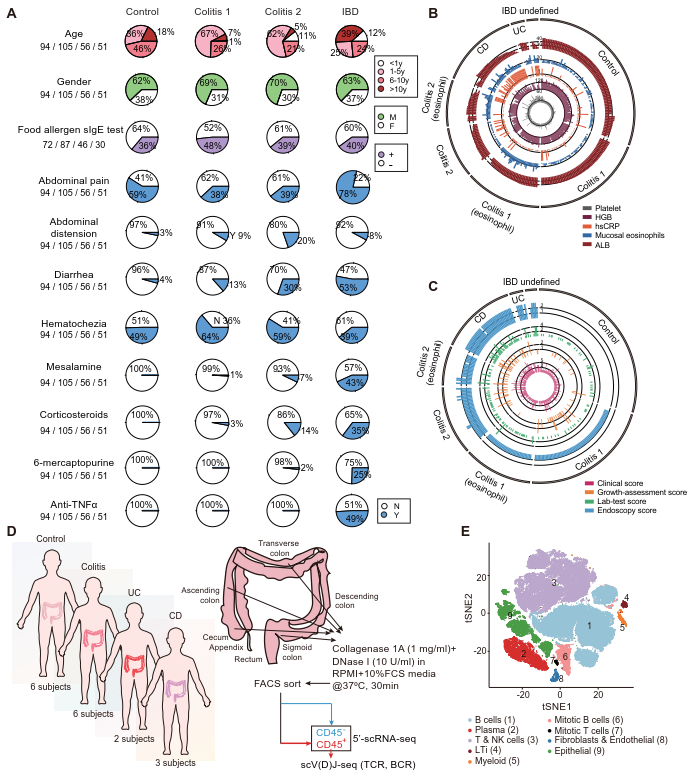
图1 队列特征与结肠黏膜单细胞图谱
2. 肠上皮细胞富集风险基因
单细胞测序将肠上皮细胞分为了10个亚群,风险基因富集在不同的细胞亚群上,发挥的功能不尽相同(图2)。比如CASP7可能引起肠上皮(coloncytes)凋亡; 可能通过catenin/WNT通路影响上皮细胞的再生;表达在Goblet细胞上的离子通道PIEZO1可能对周围的力学环境比较敏感(图2D-F)。这些蛋白的失调最终可能促进儿童结肠炎及炎症性肠病的发生发展。
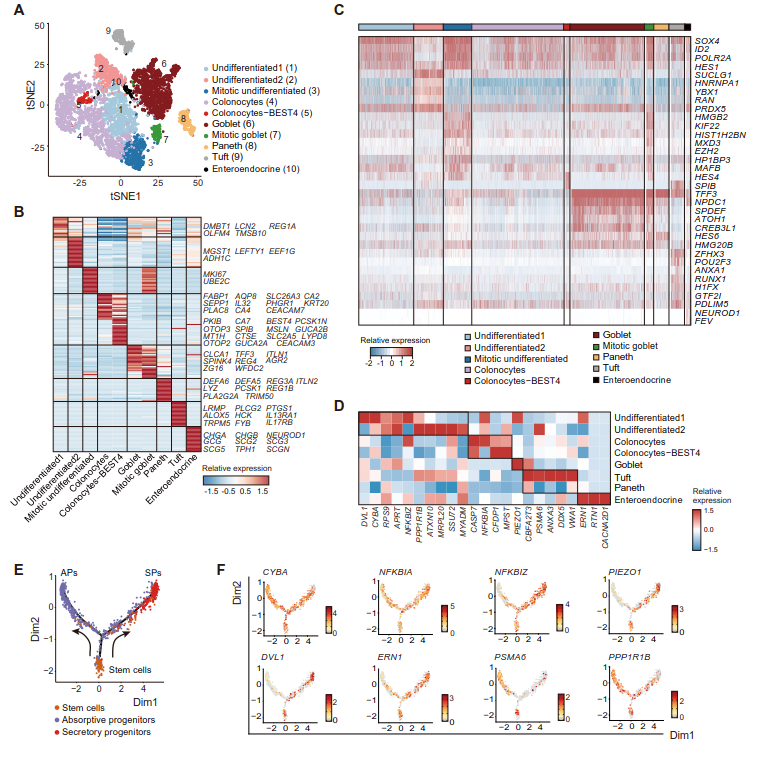
图2 PIBD与对照组结肠上皮细胞的组成与功能差异
3. 儿童结肠炎及炎症性肠病结肠黏膜富集炎性成纤维细胞且血管生成增加
结肠黏膜成纤维细胞和血管内皮细胞共有8个亚群(图3A)。PIBD的肠黏膜含有大量WNT2B高表达和炎性成纤维细胞,这些细胞富集TNFα, NF-κB和压力应答等通路,其中炎性成纤维细胞只在UC中富集(图3B-D)。PIBD中的成纤维细胞分泌更多的能招募并活化髓系细胞的CCL和CXCL家族趋化因子(图3B)。研究团队还发现疾病组的血管生成以及免疫细胞跨内皮迁移增加(图3E-F)。
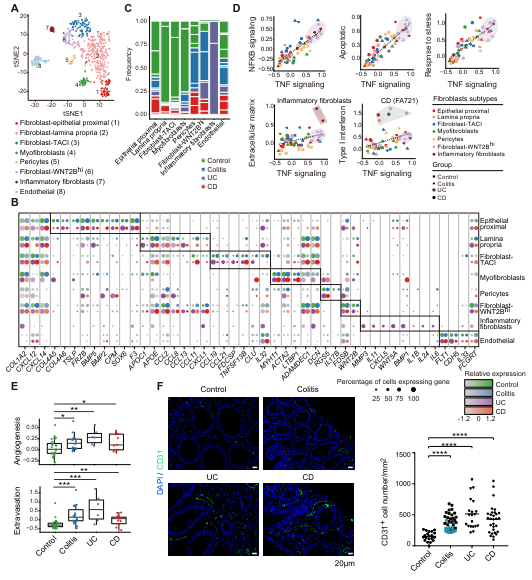
图3 PIBD与对照组的成纤维与内皮细胞组成与功能差异
4. 儿童结肠炎及炎症性肠病结肠黏膜富集高炎性髓系细胞
CD68+的髓系细胞在PIBD中,尤其是UC和CD患者中的浸润显著增加(图4A),且高表达IL1β和TNFα的巨噬细胞几乎只存在PIBD中,这类细胞中行使降解胞内cAMP功能的磷酸二酯酶4B(PDE4B)表达升高(图4B-F)。抑制PDE4B可以降低炎症因子的释放,研究团队通过体外细胞实验证实靶向PDE4B的临床药物双嘧达莫可以显著抑制TNFα,IL1β和IL6的释放(图4G-I)。
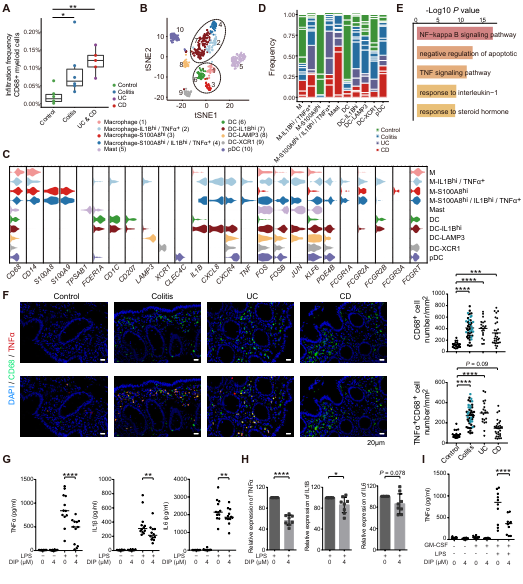
图4 PIBD结肠黏膜富集炎性髓系细胞
5. 结肠黏膜CD39缺乏诱导血小板活化和5-羟色胺累积
结合单细胞测序和免疫细胞表型分析,研究团队描述了不同T亚群的克隆扩增及转化情况(图5A-F)。值得关注的是,细胞表面表达的核酸外切酶CD39在CD8+和Vδ1+T细胞的表达在PIBD各亚型中显著降低(图5G)。CD39受cAMP-PKA-ERK-ATF2/CREB调控,可以降解胞外的ATP和ADP,研究团队证实CD39表达缺失确实会导致肠黏膜ADP浓度增加,从而激活血小板促进5-羟色胺的释放,最终诱导黏膜损伤;也通过体外细胞实验证实了靶向PDE4B的临床药物双嘧达莫可以提高Navie CD8+T细胞的CD39表达(图5H-I),这与单细胞转录组分析及过往报道提示提高cAMP可能促进CD39的表达相符。

图5 PIBD结肠黏膜缺乏CD39+的上皮T淋巴细胞
6. 双嘧达莫在防治儿童结肠炎及炎症性肠病方面的应用前景
为了证实第二信使激动剂在治疗PIBD的应用潜力,研究团队利用腹腔注射双嘧达莫的方式对硫酸葡聚糖(DSS)诱导的急性肠炎小鼠进行了治疗,发现双嘧达莫可以显著改善小鼠的体重、结肠长度和结肠的组织病理结构,抑制小鼠结肠黏膜的血小板聚集和TNFα的释放(图6A-D)。对9例患儿(8例结肠炎和1例未定型IBD)开展了双嘧达莫的小队列临床试验,发现患者的血小板计数,结肠镜评分和临床综合评分均有明显改善(图6E)。其可能的机制是双嘧达莫通过cAMP-PKA-ERK-ATF2/CREB途径提高CD39的表达,从而抑制血小板的聚集和活化(图6F-G);同时,该药可以抑制CD68+髓系细胞及TNFα的释放(图6H),最终缓解临床症状。
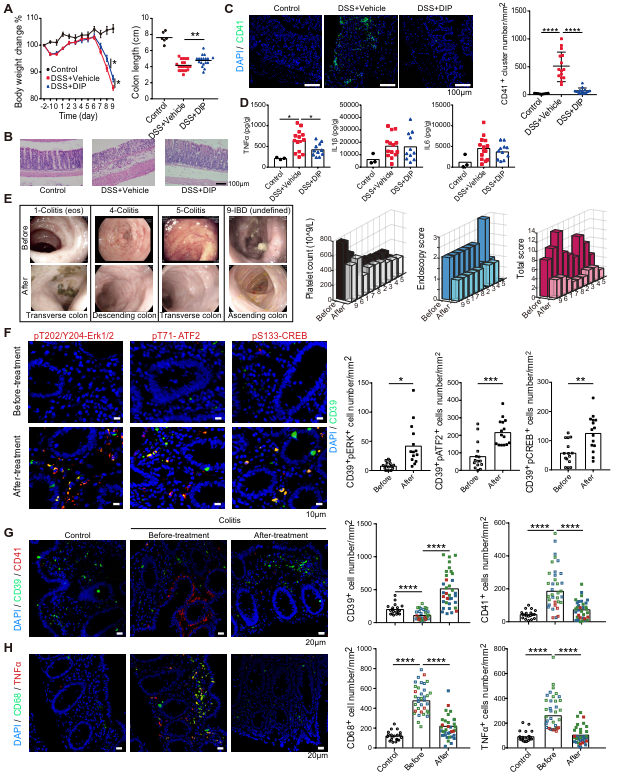
图6 双嘧达莫在临床上可以缓解结肠炎
总结
研究团队利用深度免疫分型并结合单细胞转录组测序技术、全基因组关联分析(GWAS)、体外、动物实验和临床测试,揭示了结肠炎和炎症性肠病患儿肠黏膜多个细胞亚型中的cAMP通路被抑制,从而导致级联免疫紊乱并最终促进了PIBD的发生发展(图7)。本文还发现了胞内第二信使激动剂双嘧达莫可以提高cAMP,增加CD39的表达,抑制炎性因子分泌和血小板活化,从而为儿童结肠炎及炎症性肠病的防治开拓了新的领域(图7)。未来,此类药物可能会成为儿童和/或成人胃肠炎症疾病的另一种临床防治选择,有助于降低医疗成本,促进社会和谐。但是因临床环境较为复杂,潘生丁的使用需要继续进行临床实验。具体用药请咨询临床医生。
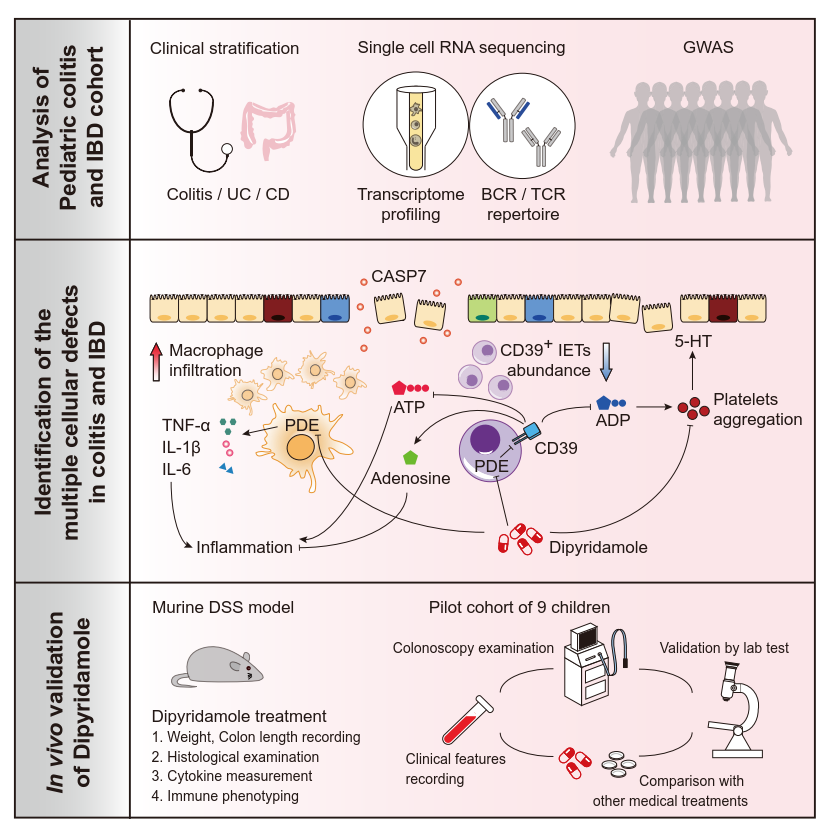
图7 本课题的技术路线与致病机制
广州医科大学附属广州市妇女儿童医疗中心儿科研究所黄冰博士,北京大学生物医学前沿创新中心的陈章华博士研究生,以及广州医科大学附属广州市妇女儿童医疗中心儿科研究所的王俊副研究员,消化科耿岚岚主任医师和数据中心梁会营主任为本文的并列第一作者,张玉霞、杨敏、白凡和龚四堂为本文的共同通讯作者。
合作团队声明本文所述实验,均经过广州医科大学附属广州市妇女儿童医疗中心伦理委员会,中国临床试验注册中心,以及广州医科大学动物实验伦理委员会的批准和通过,并严格按照批件所述的要求和流程实施。实验所涉及的遗传数据遵循国家管理办法进行储存和备案。
原文链接:https://www.cell.com/cell/fulltext/S0092-8674(19)31177-8
——————————————————
白凡简介:
北京大学生物医学前沿创新中心、生命科学学院研究员,博士生导师,国家自然科学基金委优秀青年基金获得者。2003年本科毕业于北京大学物理系,2008年获英国牛津大学生物物理博士学位。全职回国之后,白凡实验室致力于将先进的单细胞技术应用于重大医学疾病问题的研究,在癌症转移和异质性研究领域和细菌抗生素耐药研究领域取得多项重大研究成果,已在Science, Nature, Cell, Cancer Cell, Molecular Cell, PNAS等著名学术期刊发表论文60余篇。



